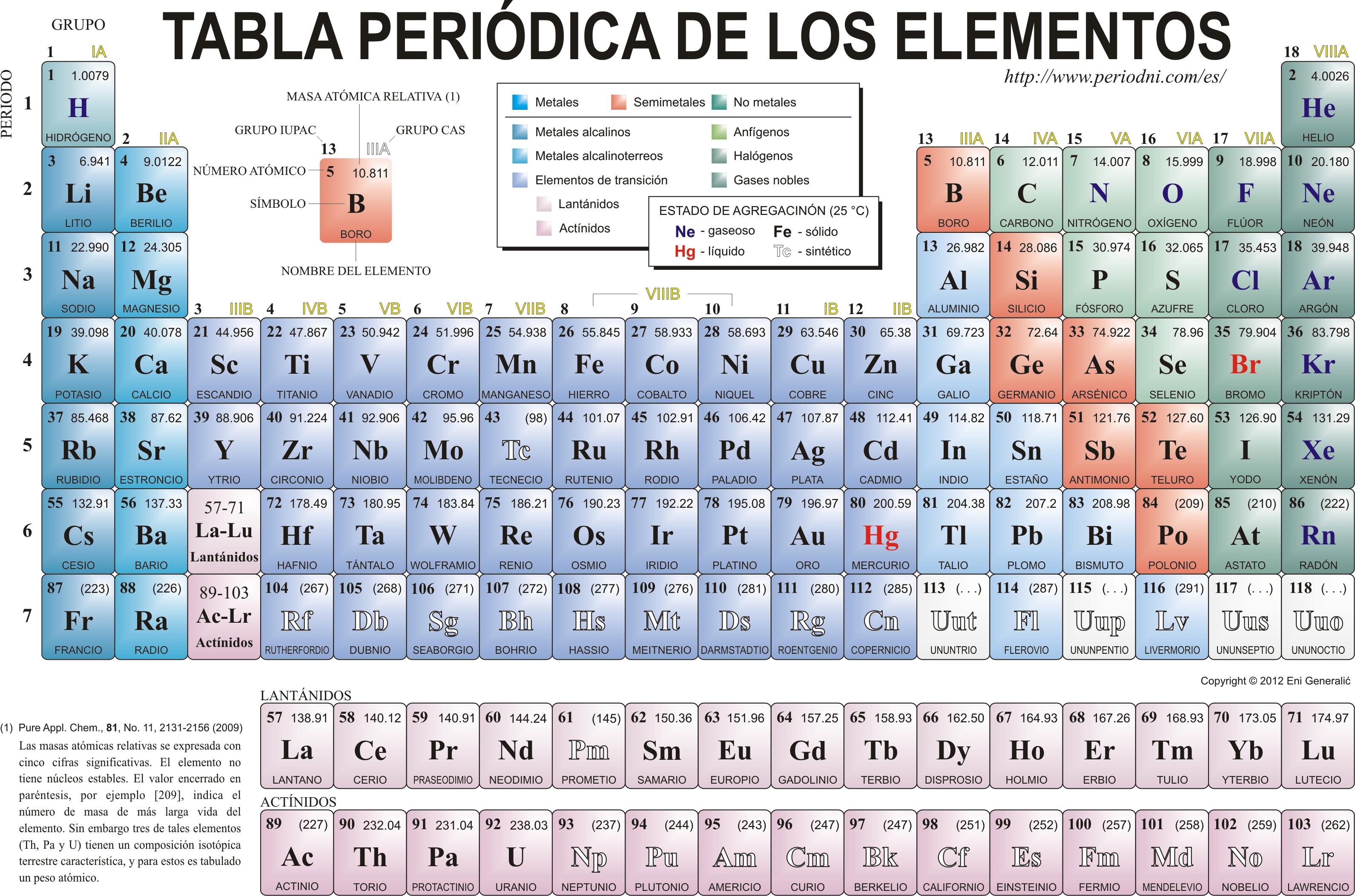
Cómo está organizada la tabla periódica


En 1869, el químico ruso Dimitri Ivánovich Mendeleiev ideó una forma de clasificar todos los elementos químicos que aparecen en la naturaleza. Este método de clasificación es la tabla periódica y muchos lo describen como el "corazón de la química". La tabla periódica nació con solo 63 elementos químicos pero, conforme fueron descubriéndose, numerosos elementos químicos se añadieron a sus filas.
En esta lección de unPROFESOR revisaremos cómo está organizada la tabla periódica, viendo qué criterios se siguen a la hora de poner los diferentes elementos en las casillas de esta tabla.
- Organización de la tabla periódica
- Grupos de elementos químicos de la tabla periódica
- Periodos de la tabla periódica
- Bloques en la tabla periódica
- Qué es la tabla periódica
- Cómo se clasifican los elementos de la tabla periódica
- Cuántos elementos tiene la tabla periódica
- Importancia de la tabla periódica
Organización de la tabla periódica
Los elementos de la tabla periódica se ordenan siguiendo diferentes parámetros:
- Los elementos aparecen en filas con orden ascendente de su número atómico, es decir, el primer elemento de la tabla periódica (hidrógeno), situado arriba a la izquierda, tiene menor número de protones (1) que el último elemento de la tabla periódica (oganesón), situado abajo a la derecha (118). A las filas de la tabla periódica se les llama periodos. De esta forma, los elementos del mismo periodo tienen una masa creciente y el mismo número de capas de electrones (número de orbitales). Estos elementos tienen patrones o tendencias similares en radio atómico, energía de ionización, afinidad electrónica y electronegatividad. Un ejemplo son el helio y el hidrógeno: ambos pertenecen al primer periodo y tiene un solo orbital electrónico, pequeño tamaño, etc.
- Los elementos que aparecen en una misma columna tienen la misma valencia química, es decir, el mismo número de electrones en su última capa. Las columnas de la tabla periódica se denominan grupos y, elementos del mismo grupo (en la misma columna) tienen la misma valencia y propiedades químicas parecidas. Un ejemplo son el litio y el sodio: ambos pertenecen al grupo 1 (primera columna) y tienden a ceder un electrón con facilidad; en cambio, el helio y el neón pertenecen al grupo 18 (es decir, la última columna) y tienen su última capa de electrones llena (capa de valencia), por lo que no ganan o ceden electrones con facilidad.
- Dentro de la tabla periódica también podemos encontrar diferentes bloques, normalmente representados en diferentes colores. Estos bloques vienen determinados por secuencia la que se llenan las capas u orbitales de electrones de los elementos. Los diferentes orbitales admiten diferente número de electrones: el orbital "s" admite 2 electrones y, una vez se llena, los electrones pasan a la siguiente capa que puede ser otro orbital "s", un orbital "p", que admite 6 electrones, etc. Así, los electrones de los elementos químicos van llenando diferente número de capas s, p, d y/o f. Cada bloque se denomina según el orbital en el que reside el último electrón: s, p, d y f.

Grupos de elementos químicos de la tabla periódica
A las columnas de la tabla periódica se les ha llamado grupos. Actualmente, en la tabla periódica que se utiliza normalmente, es decir, la estándar hay 18 grupos, numerados de izquierda a derecha del 1 al 18. Esta forma de nombrar los grupos (nomenclatura) puede variar: en ocasiones se utiliza una nomenclatura mezcla de números romanos y letras, en otras ocasiones los grupos tienen nombres comunes (metales alcalinos, halógenos, gases nobles, etc.) y en otras se nombran como "el grupo de..." y el nombre de su primer miembro (por ejemplo, "el grupo de escandio" para el grupo 3).
Elementos de un mismo grupo pueden tener patrones de diferentes propiedades:
- Aumento de radio atómico, de arriba a abajo en un grupo. Conforme descendemos en la tabla periódica, va aumentando el número de electrones y por tanto el número de capas llenas de estos. Por tanto, los electrones de la última capa (capa de valencia) se encuentran más lejos del núcleo y los átomos van siendo cada vez más grandes es decir, tienen un mayor radio.
- Desde la parte superior, cada elemento va teniendo una energía de ionización más baja. Al haber más electrones, aquellos que se encuentran en la capa de valencia están más alejados del núcleo y por tanto este los atrae con menor fuerza, haciendo que sea más fácil quitar electrones conforme descendemos en la tabla periódica.
- Finalmente, también observamos una disminución de electronegatividad dentro del mismo grupo. Nuevamente, al ser la distancia cada vez mayor entre los electrones de valencia y el núcleo, los electrones de otros átomos están más lejos de la fuerza atrayente del núcleo y por tanto este los atrae con menos fuerza que los átomos más pequeños (grupos superiores).
Estas regularidades son tendencias, es decir, hay ciertas excepciones como por ejemplo lo que ocurre en el grupo 11, donde la electronegatividad aumenta más abajo en el grupo. Además, en algunas partes de la tabla periódica como los bloques d y f, las similitudes horizontales entre elementos del mismo grupo no son tan marcadas.

Periodos de la tabla periódica
Las siete filas horizontales de la tabla periódica se llaman períodos. El número de niveles de energía de un átomo determina el periodo al que pertenece. Cada nivel está dividido en distintas categorías llamados capas u orbitales electrónicos que pueden ser de tipo s, p, d y f.
Al igual que lo que ocurría en los grupos, los elementos del mismo período tienen patrones similares de radio atómico, energía de ionización, afinidad electrónica y electronegatividad:
- En un período, el radio atómico normalmente desciende si nos movemos hacia la derecha en la tabla periódica. Conforme vamos pasando de un elemento al siguiente, se añaden protones y electrones, lo que provoca que los electrones sean arrastrados hacia el núcleo (recuerda que los electrones son muy livianos para la fuerza atractora del núcleo).
- La disminución del radio atómico en un mismo periodo hace que la energía de ionización y la electronegatividad se incremente de izquierda a derecha, ya que la atracción que ejerce el núcleo sobre los electrones es cada vez mayor.
- La afinidad electrónica también muestra un patrón a lo largo del periodo, aunque más leve. Los metales, que se encuentran a la izquierda de la tabla periódica, generalmente tienen una afinidad menor que los no metales, que están a la derecha del período. Esto es una generalidad y no se cumple para los gases nobles, que tienen su última capa (capa de valencia) llena y por tanto son muy poco reactivos.

Bloques en la tabla periódica
Los elementos de la tabla periódica se puede dividir en bloques según el orden en el que se completan las capas de electrones de los elementos. Cada bloque se nombra según el último orbital en el que, en teoría, está el último electrón (s, p, d o f):
- El bloque s está formado por los dos primeros grupos, el hidrógeno y el helio.
- El bloque p está formado por los últimos seis grupos (grupos del 13 al 18).
- El bloque d está formado los grupos 3 a 12 (comúnmente llamados metales de transición).
- El bloque f, que normalmente se coloca separado, debajo del resto de la tabla periódica, no tiene números de grupo y se compone de lantánidos y actínidos.
La tabla periódica de los elementos ha sobrevividos durante tantos años porque es un sistema que se ha demostrado muy útil y sobretodo porque se puede actualizar. En teoría, podría haber más elementos que llenarían otros orbitales, pero estos todavía no se han sintetizado o no se han descubierto. En el caso en que se descubrieran nuevos elementos atómicos, los investigadores continuarían con el orden alfabético para nombrar los diferentes bloques (bloque g, bloque h, etc.).

Qué es la tabla periódica
La tabla periódica de los elementos es una herramienta imprescindible en la química. Es una tabla que reúne todos los elementos químicos conocidos, mostrándolos de forma ordenada según su número atómico (es decir, la cantidad de protones en el núcleo de cada átomo), su configuración electrónica y sus propiedades químicas.
Fue creada en el siglo XIX por el químico ruso Dmitri Mendeléyev, quien se dio cuenta de que muchos elementos compartían características similares y que estas propiedades se repetían de forma periódica. Con esa idea en mente, propuso organizar los elementos en una tabla, dejando incluso huecos para aquellos que todavía no se habían descubierto. Con el tiempo, su intuición se vio confirmada y la tabla se fue completando y perfeccionando.
Hoy en día, la tabla periódica no funciona como un listado, sino que es una guía visual que permite predecir cómo se comporta un elemento, con qué otros puede reaccionar, si forma ácidos, bases o sales, y qué tipo de enlaces químicos puede establecer.
Cómo se clasifican los elementos de la tabla periódica
La tabla periódica está estructurada en filas y columnas que reflejan algunos patrones repetitivos (o “periódicos”) de las propiedades químicas. Esta clasificación se hace a través de cuatro grandes criterios: períodos, grupos, bloques y tipo de elemento.
1. Períodos
Son las filas horizontales de la tabla. Hay 7 períodos en total. Cada nuevo período indica que los elementos tienen una capa de electrones más con respecto al anterior. Por ejemplo, el sodio (Na) está en el tercer período porque sus electrones ocupan hasta tres niveles de energía.
2. Grupos
Los grupos son las columnas verticales, también llamadas familias. Hay 18 grupos, y los elementos de un mismo grupo tienen propiedades similares porque poseen el mismo número de electrones de valencia (los de la capa más externa del átomo). Por ejemplo, el grupo 1 contiene a los metales alcalinos, que todos tienen un solo electrón de valencia y son altamente reactivos.
3. Bloques
La tabla también se divide en bloques s, p, d y f, dependiendo del tipo de orbital en el que se encuentran los últimos electrones del átomo. Esto nos habla de la configuración electrónica de cada uno de los elementos:
Bloque s: grupos 1 y 2 + helio.
Bloque p: grupos 13 al 18.
Bloque d: los metales de transición, en el centro (grupos 3 al 12).
Bloque f: lantánidos y actínidos, que suelen aparecer en dos filas separadas abajo.
4. Tipo de elemento
Los elementos también se agrupan por sus propiedades físico-químicas en:
Metales: buenos conductores de electricidad y calor, brillantes, maleables. Ocupan la parte izquierda y central.
No metales: malos conductores, frágiles o gaseosos. Están en la parte superior derecha.
Metaloides: tienen propiedades intermedias. Forman una línea diagonal entre los metales y no metales.
Cuántos elementos tiene la tabla periódica
La tabla periódica moderna contiene 118 elementos, según la IUPAC (Unión Internacional de Química Pura y Aplicada). Estos elementos se pueden clasificar de la siguiente manera:
94 elementos existen en la naturaleza, es decir, pueden encontrarse de forma natural en la Tierra o el universo.
24 elementos han sido sintetizados artificialmente en laboratorios, a través de aceleradores de partículas. Estos elementos no se encuentran en condiciones naturales y muchos de ellos son radiactivos y de vida muy corta.
Cada elemento tiene un nombre, un símbolo químico (como H para hidrógeno o O para oxígeno), un número atómico y una masa atómica. También se suele indicar su estado de agregación (sólido, líquido o gas) en condiciones normales de temperatura y presión.
Los elementos más nuevos, como el oganesón (Og) o el teneso (Ts), fueron confirmados oficialmente en la última década. Aunque no se tienen todos los conocimientos acerca de estos nuevos elementos, su incorporación a la tabla confirma que esta herramienta es un sistema abierto, en constante evolución.
Importancia de la tabla periódica
La tabla periódica es uno de los mayores logros de la ciencia: una herramienta viva, en constante crecimiento, que organiza de forma lógica y funcional todos los elementos conocidos. Esta tabla ayuda a los químicos a entender la materia, pero además guía la innovación científica y tecnológica en muchas otras disciplinas. Entender su estructura, su lógica y su utilidad es básico para cualquier persona que quiera conocer cómo está hecho el universo… o simplemente para aprobar la asignatura de química.
La tabla periódica es una herramienta de organización y predicción que tiene aplicaciones prácticas en ciencia, tecnología, medicina, ingeniería, industria y hasta en la vida cotidiana. A continuación, te presentamos algunas de las razones por las que es importante la tabla periódica.
Facilita el estudio de la química
Permite aprender con mayor facilidad las propiedades de los elementos sin memorizarlos uno a uno. Gracias a la organización por grupos, se puede predecir cómo reaccionará un elemento con otro.
Predice propiedades de los elementos desconocidos
Cuando se descubren nuevos elementos, su posición en la tabla nos permite anticipar cómo se comportarán. Eso fue lo que hizo Mendeléyev con el germanio, que predijo como "eka-silicio" años antes de su descubrimiento.
Ayuda a entender las reacciones químicas
Saber cuántos electrones tiene un elemento en su capa de valencia permite predecir si va a donar, aceptar o compartir electrones, y con qué facilidad puede formar compuestos.
Es importante en el desarrollo de materiales y tecnologías
Desde baterías de litio, pasando por aleaciones resistentes al calor hasta medicamentos con compuestos halogenados, todo parte del conocimiento profundo de las propiedades de los elementos que se resume en la tabla periódica.
Es útil en otros sectores además de la química
La biología molecular, la nanotecnología, la geología o la astrofísica también usan la tabla para identificar componentes de organismos, minerales o cuerpos celestes.
Si deseas leer más artículos parecidos a Cómo está organizada la tabla periódica, te recomendamos que entres en nuestra categoría de El átomo.
- Scerri, E. R. (2008). La tabla periódica. Investigación y ciencia, 50-56.
- Valderrama, B. (2018). La rueda de motivos: hacia una tabla periódica de la motivación humana. Papeles del psicólogo, 39(1), 60-70.